在藥品生產(chǎn)質(zhì)量管理規(guī)范(GMP)日益嚴(yán)格的全球背景下,計(jì)算機(jī)化系統(tǒng)驗(yàn)證(CSV)已成為確保制藥企業(yè)生產(chǎn)數(shù)據(jù)完整性、產(chǎn)品質(zhì)量與合規(guī)性的核心環(huán)節(jié)。GAMP5(良好自動(dòng)化生產(chǎn)實(shí)踐指南第5版)作為國(guó)際公認(rèn)的計(jì)算機(jī)化系統(tǒng)生命周期管理框架,為我國(guó)制藥企業(yè)提供了系統(tǒng)化、風(fēng)險(xiǎn)導(dǎo)向的驗(yàn)證方法論。本文旨在探討基于GAMP5的計(jì)算機(jī)化系統(tǒng)驗(yàn)證在我國(guó)制藥企業(yè)的應(yīng)用現(xiàn)狀、挑戰(zhàn)及優(yōu)化路徑,以促進(jìn)產(chǎn)業(yè)升級(jí)與合規(guī)水平提升。
一、GAMP5框架的核心原則與驗(yàn)證流程
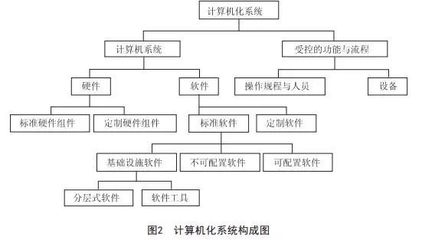
GAMP5框架強(qiáng)調(diào)“基于風(fēng)險(xiǎn)、生命周期管理、供應(yīng)商參與”三大支柱,將計(jì)算機(jī)化系統(tǒng)驗(yàn)證融入從概念到退役的全過程。其核心流程包括:
- 分類與風(fēng)險(xiǎn)評(píng)估:根據(jù)系統(tǒng)復(fù)雜性與影響程度(如直接影響產(chǎn)品質(zhì)量的GxP系統(tǒng)),確定驗(yàn)證深度與范圍。
- 生命周期管理:涵蓋用戶需求說明(URS)、設(shè)計(jì)確認(rèn)(DQ)、安裝確認(rèn)(IQ)、運(yùn)行確認(rèn)(OQ)、性能確認(rèn)(PQ)等階段,確保系統(tǒng)始終處于受控狀態(tài)。
- 供應(yīng)商管理:利用供應(yīng)商評(píng)估與文檔支持,降低自開發(fā)系統(tǒng)的驗(yàn)證負(fù)擔(dān)。
二、我國(guó)制藥企業(yè)計(jì)算機(jī)化系統(tǒng)驗(yàn)證的應(yīng)用現(xiàn)狀
隨著《藥品生產(chǎn)質(zhì)量管理規(guī)范(2010年修訂)》及附錄《計(jì)算機(jī)化系統(tǒng)》的發(fā)布,我國(guó)制藥企業(yè)已普遍啟動(dòng)CSV實(shí)踐,但應(yīng)用水平參差不齊:
- 優(yōu)勢(shì)領(lǐng)域:大型跨國(guó)或領(lǐng)先本土企業(yè)在ERP、MES、LIMS等核心系統(tǒng)驗(yàn)證中,已逐步采用GAMP5框架,形成標(biāo)準(zhǔn)化流程,并借助自動(dòng)化工具提升效率。
- 普遍挑戰(zhàn):中小型企業(yè)常面臨資源有限、專業(yè)人才缺乏、驗(yàn)證文檔形式化等問題。部分企業(yè)將驗(yàn)證視為“一次性合規(guī)任務(wù)”,忽視持續(xù)監(jiān)控與變更控制,導(dǎo)致系統(tǒng)后期運(yùn)維風(fēng)險(xiǎn)升高。
- 技術(shù)痛點(diǎn):對(duì)云計(jì)算、物聯(lián)網(wǎng)等新興技術(shù)的驗(yàn)證經(jīng)驗(yàn)不足,傳統(tǒng)驗(yàn)證方法難以完全適應(yīng)敏捷開發(fā)與持續(xù)交付模式。
三、基于GAMP5的優(yōu)化實(shí)踐路徑
為提升驗(yàn)證效能與合規(guī)水平,我國(guó)制藥企業(yè)可聚焦以下方向:
- 建立風(fēng)險(xiǎn)導(dǎo)向的驗(yàn)證策略:依據(jù)系統(tǒng)GxP影響分級(jí),差異化配置驗(yàn)證資源。例如,對(duì)高風(fēng)險(xiǎn)的工藝控制系統(tǒng)實(shí)施全生命周期驗(yàn)證,而對(duì)低風(fēng)險(xiǎn)的辦公軟件采用簡(jiǎn)化流程。
- 強(qiáng)化供應(yīng)商協(xié)作與文檔復(fù)用:優(yōu)先選擇符合GAMP5標(biāo)準(zhǔn)的供應(yīng)商,利用供應(yīng)商提供的驗(yàn)證包(如設(shè)計(jì)文檔、測(cè)試案例)減少重復(fù)工作,同時(shí)通過審計(jì)確保其質(zhì)量體系可靠性。
- 推動(dòng)驗(yàn)證流程自動(dòng)化與數(shù)字化:引入專用CSV管理軟件或集成式平臺(tái),實(shí)現(xiàn)需求追蹤、測(cè)試執(zhí)行、缺陷管理、文檔生成的自動(dòng)化,降低人為錯(cuò)誤并提升可追溯性。
- 培育專業(yè)人才與合規(guī)文化:通過內(nèi)訓(xùn)、行業(yè)交流及第三方服務(wù)合作,構(gòu)建既懂GMP又熟悉IT技術(shù)的復(fù)合型團(tuán)隊(duì),并將驗(yàn)證意識(shí)融入日常運(yùn)維與變更管理。
- 適應(yīng)新技術(shù)與敏捷模式:針對(duì)云部署、AI分析等系統(tǒng),在GAMP5靈活框架下探索“迭代驗(yàn)證”與“持續(xù)驗(yàn)證”方法,結(jié)合敏捷開發(fā)周期嵌入驗(yàn)證活動(dòng),確保合規(guī)性與創(chuàng)新平衡。
四、結(jié)論與展望
GAMP5框架為我國(guó)制藥企業(yè)計(jì)算機(jī)化系統(tǒng)驗(yàn)證提供了科學(xué)且適應(yīng)性強(qiáng)的指南。隨著監(jiān)管要求的細(xì)化與工業(yè)4.0技術(shù)的滲透,企業(yè)需進(jìn)一步將驗(yàn)證從“合規(guī)驅(qū)動(dòng)”轉(zhuǎn)向“質(zhì)量與效率驅(qū)動(dòng)”,通過標(biāo)準(zhǔn)化、自動(dòng)化與智能化手段,構(gòu)建穩(wěn)健的計(jì)算機(jī)化系統(tǒng)治理體系。這不僅有助于通過國(guó)內(nèi)外GMP審計(jì),更能為藥品全生命周期數(shù)據(jù)可靠性與患者安全奠定堅(jiān)實(shí)基礎(chǔ),最終推動(dòng)我國(guó)制藥行業(yè)的高質(zhì)量發(fā)展。